Впервые вживую визуализирован фундаментальный механизм памяти

Исследователи смогли воочию наблюдать изменения в нейронах, связанные с памятью. Это открытие, сделанное в Нидерландском институте нейронаук, показывает, как нейроны адаптируют свою форму для укрепления связей. Исследование подчеркивает пластичность начального участка аксона и его роль в регуляции памяти. Эти открытия могут повлиять на исследования неврологических расстройств, связанных с памятью.
Память — фундаментальная способность хранить и вспоминать информацию — играет центральную роль в нашей личности и человеческом опыте. Несмотря на то, что ее сложная природа изучается уже несколько десятилетий, многое еще предстоит узнать о точных механизмах, лежащих в ее основе.
Недавно исследователи из Нидерландского института нейронаук сделали значительный шаг вперед, визуализировав в реальном времени процесс, важный для формирования памяти. Это открытие, связанное с тем, как нейроны изменяют свою форму для укрепления связей, может пролить свет на наше понимание биологических основ памяти. Результаты исследования опубликованы в журнале .
Пластичность начального сегмента аксона
В основе этого открытия лежит начальный сегмент аксона (AIS) - специфическая часть нейрона. Пластичность AIS, т.е. его способность изменяться в зависимости от активности нейрона, играет важнейшую роль в способе передачи информации нейронами. Более конкретно, эта пластичность позволяет нейронам регулировать свой ответ, или потенциал действия, в зависимости от изменений активности нейронной сети.
Нора Джаманн, соавтор исследования, в своем пресс-релизе отмечает: "Когда вы учитесь, активность нейронной сети постоянно колеблется. Нейроны должны функционировать в условиях экстремальных колебаний уровня активности: слишком низкая или слишком высокая активность может препятствовать формированию памяти". Авторы объясняют, что предыдущие эксперименты на мышах проиллюстрировали эту способность к адаптации: мышь с отрезанными усами получает уменьшенный сенсорный вход. В результате количество натриевых каналов в AIS увеличивается для поддержания равновесия.
Обратный эффект также имеет место: при избытке входного сигнала, например, когда мышь помещается в новую среду с высокой активностью, AIS становится немного короче и содержит меньше натриевых каналов. Но как это происходит и как быстро возникает эта пластичность, всегда было фундаментальным вопросом для нейробиологов.
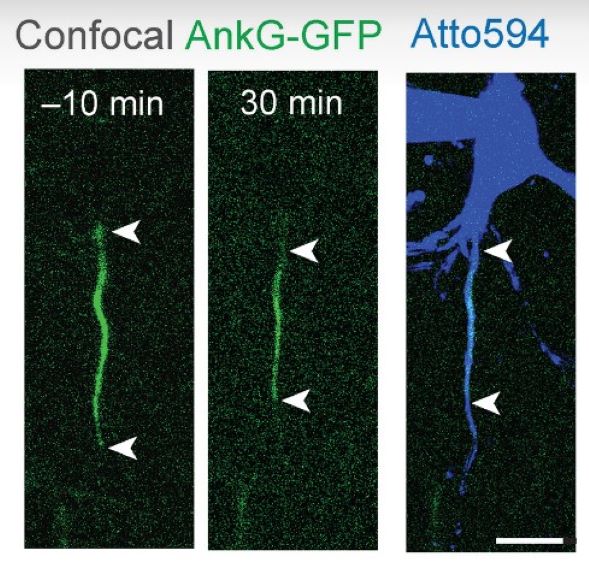
Визуализация в реальном времени
Амели Фреаль говорит: "Чтобы ответить на этот вопрос, мы столкнулись с серьезной проблемой: как запечатлеть пластичность в реальном времени? Если вам интересно, как адаптируется AIS, вы хотите увидеть, как она движется. Раньше это было невозможно в полевых условиях. В данном исследовании мы использовали два новых инструмента".
Во-первых, авторы использовали специальную модель мыши с AIS, меченной флуоресцентным белком, что позволило наблюдать механизм и регистрировать временные изменения в срезах мозга. Они также использовали молекулярные инструменты, чтобы сделать натриевые каналы видимыми в клеточных культурах. Это впервые позволило наблюдать за работой натриевых каналов вживую.
Роль натриевых каналов в коммуникации между нейронами
В исследовании подробно описаны молекулярные механизмы работы. Активация рецептора N-метил-D-аспартата (NMDA), специфического белка, присутствующего в нейронах, приводит к серьезным явлениям, в том числе к длительной синаптической депрессии, т.е. к снижению эффективности передачи информации между нейронами.
Конкретно исследователи наблюдали быструю интернализацию (эндоцитоз) натриевых каналов, присутствующих в AIS. Эти каналы, обеспечивающие прохождение ионов натрия, необходимы для генерации потенциалов действия в нейронах. При стимуляции нейрона эти каналы открываются, пропуская ионы натрия внутрь клетки. Это быстрое проникновение вызывает быстрое изменение электрической полярности клетки, генерируя так называемый потенциал действия. Именно этот потенциал действия распространяется по нейрону и обеспечивает передачу информации.
Инициация потенциала действия является тонко регулируемым процессом. Натриевые каналы, открываясь и закрываясь, определяют, когда и как именно генерируется потенциал действия.
В контексте дистальной AIS эндоцитоз натриевых каналов означает, что эти каналы удаляются из данной конкретной области нейрона. При уменьшении количества доступных натриевых каналов нейрону требуется более сильная стимуляция для возникновения потенциала действия. Это изменение порога генерации потенциала действия влияет на способ связи нейронов друг с другом и, следовательно, на способ обработки и передачи информации в мозге.
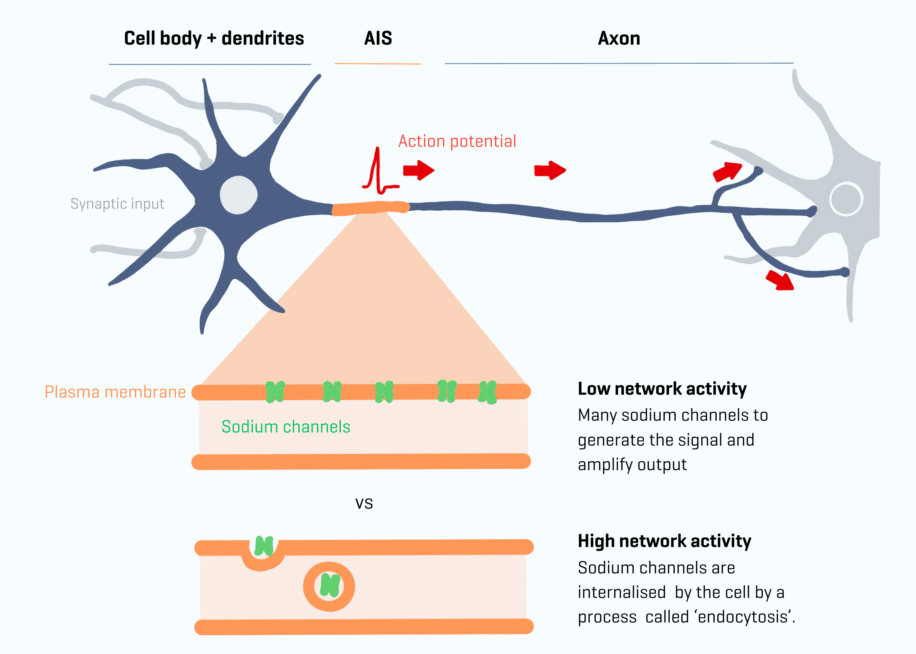
Последствия для исследований памяти
Более глубокое понимание этих структурных и функциональных изменений позволяет исследователям расширить свои знания о механизмах, обеспечивающих получение, хранение и запоминание информации в мозге.
Эти открытия также открывают новые терапевтические перспективы. Нарушения памяти, связанные с нейродегенеративными заболеваниями, такими как болезнь Альцгеймера, повреждениями мозга или другими состояниями, могут иметь различное происхождение. Однако результаты исследования открывают возможность более точного воздействия на дисфункции, лежащие в основе этих нарушений.
Выяснив, как нейроны адаптируют свою форму и функции, можно разработать вмешательства, стимулирующие, модулирующие или восстанавливающие эти адаптивные механизмы. Будь то фармакологические подходы, неинвазивные вмешательства, такие как транскраниальная магнитная стимуляция, или другие методы, такое углубленное понимание может привести к более эффективному и целенаправленному лечению расстройств памяти.